
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
复星医药
600196 |
1.4%
|
最新:25.36
开盘:25.29 昨收:25.01 |
开盘%:1.12%
振幅%:1.48% 换手%:0.42% |
最高:25.5
最低:25.13 量比:0.74 |
总市值:677 亿
流通值:537 亿 成交额:21 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
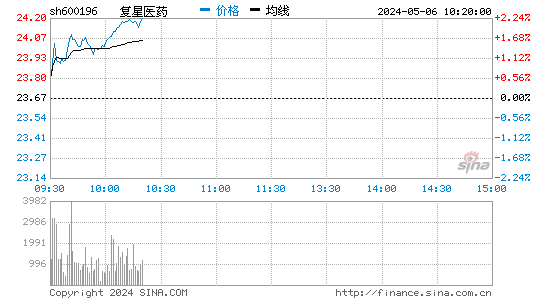
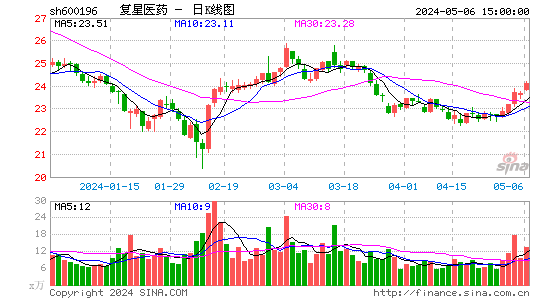
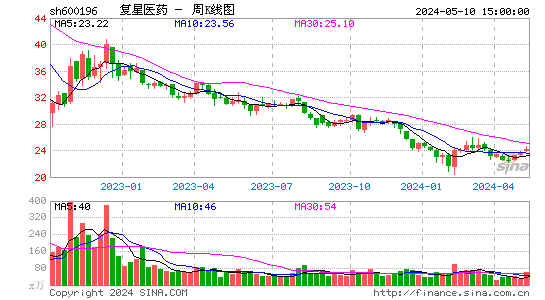
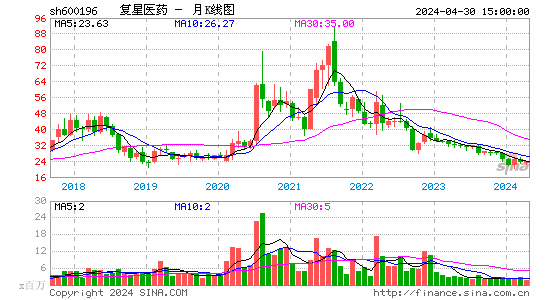
复星医药股票概况
了解全球化医药健康产业集团的股市表现
一、公司概况
复星医药(600196.SH,02196.HK)成立于1994年,是一家植根中国、创新驱动的全球化医药健康产业集团。其业务范围涵盖制药、医疗器械与医学诊断、医疗健康服务等领域,并通过参股国药控股扩展到医药商业领域。
二、股市表现
截至2025年2月10日,复星医药A股收盘价为25.43元,港股收盘价为14.840港元。股价呈现波动性,但整体呈现上升趋势,显示出市场对复星医药的信心。
三、主营业务
制药业务:作为公司的核心业务,包括创新药、成熟产品及制造业务、疫苗业务。其中,创新药业务聚焦肿瘤、免疫等核心治疗领域。
医疗器械与医学诊断:构建以医疗美容、呼吸健康等为核心的三大业务分支。
医疗健康服务:形成线上线下一体化的医疗服务平台。
四、财务状况
复星医药的资产负债率维持在48.64%左右,财务状况稳定。营业收入和归母净利润持续增长,显示出良好的盈利能力和销售毛利率。
五、创新与发展
复星医药在创新药方面增长动能强劲,业务结构持续优化。公司积极推动优质产品出海,不断提升国际声誉和市场份额。
总结
复星医药作为全球化医药健康产业集团的佼佼者,以其稳健的股市表现、多元化的业务布局、良好的财务状况以及持续的创新与发展,赢得了市场和投资者的广泛认可。未来,随着全球医疗健康市场的不断发展,复星医药有望继续保持强劲的增长势头。
2026-02-25 16:38
【复星医药:控股子公司药品获临床试验批准】2月25日电,复星医药(600196.SH)公告称,控股子公司复星医药产业发展有限公司收到国家药品监督管理局关于同意复迈宁®(通用名:芦沃美替尼片)联合安罗替尼用于晚期非小细胞肺癌患者开展临床试验的批准。复星医药产业拟于中国境内开展该药品的Ⅱ期临床试验。该药品为MEK1/2选择性抑制剂,已在中国境内上市并获批两项适应症。此外,该药品另有两项适应症的药品上市申请已获国家药监局受理并获纳入优先审评程序。根据IQVIA MIDAS™最新数据,2024年,MEK1/2选择性抑制剂于全球范围的销售额约为20.68亿美元。但该药品用于本次新增适应症尚需在中国境内开展一系列临床研究并经国家药品审评部门审批通过后,方可上市。药品研发存在一定风险,敬请广大投资者注意投资风险。
2026-02-12 16:44
【复星医药:控股子公司药品获临床试验批准】2月12日电,复星医药(600196.SH)公告称,公司控股子公司复宏汉霖收到国家药品监督管理局关于同意HLX15-SC(重组抗CD38全人单克隆抗体注射液-皮下注射)用于多发性骨髓瘤治疗开展Ⅰ期临床试验的批准。复宏汉霖拟在中国境内开展该药品的相关临床研究。HLX15是复星医药自主研发的达雷妥尤单抗生物类似药,包括皮下注射剂型HLX15-SC和静脉注射剂型HLX15-IV,拟用于多发性骨髓瘤等治疗。截至2026年1月,针对HLX15的累计研发投入约为人民币19,153万元。根据中国相关法规要求,HLX15尚需在中国境内开展一系列临床研究并经国家药品审评部门审批通过后,方可上市。药品研发及至上市是一项长期工作,存在诸多不确定因素,敬请广大投资者注意投资风险。
2026-02-10 16:29
【复星医药:控股子公司药品注册申请获受理】2月10日电,复星医药(600196.SH)公告称,公司控股子公司上海朝晖药业有限公司就盐酸丁卡因凝胶的药品注册申请获国家药品监督管理局受理。该药品拟用于经皮局部麻醉,适用于成人及1个月以上的婴儿。
2026-02-05 20:16
【复星医药:复迈宁新增成人NF1适应症申报上市获受理并纳入优先审评程序】2月5日,复星医药宣布公司自主研发的MEK 1/2抑制剂芦沃美替尼片(商品名:复迈宁®)用于治疗伴有症状、无法手术的丛状神经纤维瘤(PN)的Ⅰ型神经纤维瘤病(NF1)成人患者的药品上市申请获国家药监局受理并已获纳入优先审评程序。
2026-02-05 16:35
【复星医药:控股子公司药品注册申请获受理】2月5日电,复星医药(600196.SH)公告称,控股子公司吉斯美(武汉)制药有限公司就环磷酰胺注射液的药品注册申请获国家药品监督管理局受理。该药品为本集团自主研发的化学药品,拟用于治疗多种疾病。截至2025年12月,本集团针对该药品的累计研发投入约为人民币740万元。2024年,环磷酰胺注射剂在中国境内的销售额约为人民币2.91亿元。该药品在进行商业化生产前,尚需获得药品注册批准等。本次药品注册申请获受理不会对本集团现阶段业绩产生重大影响。由于医药产品的行业特点,药品上市后的具体销售情况可能受到多种因素影响,具有较大不确定性。
2026-02-05 16:35
【复星医药:控股子公司复宏汉霖与Eisai签订许可协议】2月5日电,复星医药(600196.SH)公告称,公司控股子公司复宏汉霖与Eisai签订《许可协议》,授予Eisai于日本及领域(即用于肿瘤适应症治疗)开发、生产及商业化斯鲁利单抗注射液的权利。协议包括至多15,501万美元的首付款、监管里程碑款项,以及至多23,333万美元的销售里程碑款项和特许权使用费。该合作有助于进一步拓展复星医药产品的海外市场。但药品研发具有不确定性,且相关款项的收取亦存在不确定性。
2026-02-05 16:33
复星医药:控股子公司复宏汉霖与Eisai签订《许可协议》,由复宏汉霖授予Eisai于许可区域(即日本)及领域(即用于肿瘤适应症治疗)开发、生产及商业化斯鲁利单抗注射液的权利。根据约定,Eisai应就许可产品向复宏汉霖支付至多1.55亿美元不可退还的首付款、监管里程碑款项。
2026-01-27 17:00
【复星医药:聘任孟凌媛为公司副总裁】1月27日电,复星医药(600196.SH)公告称,公司第十届董事会第二十三次会议同意聘任孟凌媛为公司副总裁,任期自2026年1月26日起至本届董事会任期届满之日止。孟凌媛曾任普华永道会计师事务所经理、高级经理,复星高科技审计高级总监等职务,拥有中国注册会计师资质。截至2026年1月26日,孟凌媛未持有公司股份,与公司不存在关联关系,也不存在不得担任上市公司高级管理人员的情形。
2026-01-27 16:55
【复星医药:控股子公司药品获临床试验批准】1月27日电,复星医药(600196.SH)公告称,公司控股子公司复宏汉霖收到国家药监局关于同意注射用HLX43联合HLX07及斯鲁利单抗注射液用于晚期实体瘤治疗开展临床试验的批准。复宏汉霖拟于条件具备后在中国境内开展该治疗方案的Ⅱ期临床研究。HLX43为复宏汉霖利用许可引进的新型DNA拓扑异构酶I抑制剂小分子毒素-肽链连接子与其自主研发的靶向PD-L1的抗体进行偶联开发的靶向PD-L1的抗体偶联药物(ADC),拟用于治疗晚期/转移性实体瘤;HLX07为复宏汉霖自主研发的针对EGFR靶点的创新型生物药,拟用于治疗晚期实体瘤;斯鲁利单抗注射液为复宏汉霖自主研发的创新型抗PD-1单抗。
2026-01-23 08:03
【复星医药:拟分拆复星安特金至香港联交所主板上市】复星医药1月22日公告,拟分拆所属子公司复星安特金至香港联交所主板上市。本次分拆完成后,复星医药的股权结构不会因此发生重大变化,且预计仍将维持对复星安特金的控制权。通过本次分拆,复星安特金将作为复星医药下属疫苗业务平台实现独立上市,借助香港资本市场拓宽融资渠道、增强资金实力,并完善激励机制,有利于其持续强化在疫苗领域的综合竞争力、品牌知名度和市场影响力。复星医药同日公告,控股子公司锦州奥鸿药业有限责任公司就重酒石酸去甲肾上腺素注射液的药品注册申请获国家药品监督管理局批准。
2026-01-22 18:24
【复星医药:拟分拆复星安特金至香港联交所主板上市】1月22日电,复星医药(600196)1月22日公告,拟分拆所属子公司复星安特金至香港联交所主板上市。本次分拆完成后,复星医药的股权结构不会因此发生重大变化,且预计仍将维持对复星安特金的控制权。通过本次分拆,复星安特金将作为复星医药下属疫苗业务平台实现独立上市,借助香港资本市场拓宽融资渠道、增强资金实力,并完善激励机制,有利于其持续强化在疫苗领域的综合竞争力、品牌知名度和市场影响力。复星医药同日公告,控股子公司锦州奥鸿药业有限责任公司就重酒石酸去甲肾上腺素注射液的药品注册申请获国家药品监督管理局批准。
2026-01-22 18:08
【复星医药:分拆所属子公司复星安特金至香港联交所主板上市获董事会批准】1月22日电,复星医药(600196.SH)公告称,公司第十届董事会第二十二次会议审议通过关于分拆所属子公司复星安特金(成都)生物制药股份有限公司至香港联交所主板上市的议案。该议案包括分拆上市符合相关法律法规规定、首次公开发行H股股票方案、分拆上市预案以及分拆上市符合《上市公司分拆规则(试行)》等内容。公司表示,本次分拆上市符合相关法律法规及监管机构的要求,具备可行性。
2026-01-22 18:08
【复星医药:控股子公司药品重酒石酸去甲肾上腺素注射液获注册批准】1月22日电,复星医药(600196.SH)公告称,公司控股子公司锦州奥鸿药业有限责任公司就重酒石酸去甲肾上腺素注射液的药品注册申请获国家药品监督管理局批准。该药品获批适应症包括急性低血压状态的血压恢复、心跳骤停的辅助治疗和心跳骤停复苏后的血压维持等。该药品为复星医药自主研发的化学药品,截至2025年12月,累计研发投入约为人民币874万元。根据IQVIA CHPA数据,2024年该药品在中国境内的销售额约为人民币18.11亿元。该药品获批上市将进一步丰富复星医药的产品线,但具体销售情况可能受到多种因素影响,具有较大不确定性。
2026-01-20 16:36
复星医药:控股子公司复宏汉霖收到国家药品监督管理局关于同意HLX701(重组人SIRPα-IgG4 Fc融合蛋白注射液)联合西妥昔单抗和化疗治疗晚期结直肠癌开展Ⅰb/Ⅱ期临床试验的批准。
2026-01-14 19:59
【复星医药:注射用乳糖酸红霉素药品注册申请获受理】1月14日电,复星医药(600196)1月14日公告,控股子公司苏州二叶制药有限公司就注射用乳糖酸红霉素的药品注册申请近期获国家药监局受理。该药品为化学药品,拟用于当口服给药不可行或感染的严重程度需要快速达到高红霉素血清浓度时,治疗由特定微生物敏感株引起的感染;预防风湿热初发;预防风湿热复发;预防细菌性心内膜炎。
2026-01-14 17:30
【复星医药:控股子公司药品注册申请获受理】1月14日电,复星医药(600196.SH)公告称,公司控股子公司苏州二叶制药有限公司就注射用乳糖酸红霉素的药品注册申请于近期获国家药品监督管理局受理。该药品为化学药品,拟用于当口服给药不可行或感染的严重程度需要快速达到高红霉素血清浓度时,用于治疗由特定微生物敏感株引起的感染;预防风湿热初发;预防风湿热复发;预防细菌性心内膜炎。
2026-01-14 10:35
【复星医药、中汇人寿等成立股权投资基金】1月14日电,企查查APP显示,近日,中汇复弘(天津)股权投资基金合伙企业(有限合伙)成立,出资额5.47亿元,经营范围为以私募基金从事股权投资、投资管理、资产管理等活动。企查查股权穿透显示,该合伙企业由中汇人寿保险股份有限公司、复星医药全资子公司上海复星医药产业发展有限公司、弘毅私募基金管理(天津)合伙企业(有限合伙)共同出资。
2026-01-13 15:14
【复星医药、中汇人寿等在天津成立股权投资基金,出资额5.47亿】天眼查工商信息显示,近日,中汇复弘(天津)股权投资基金合伙企业(有限合伙)成立,执行事务合伙人为弘毅私募基金管理(天津)合伙企业(有限合伙),出资额5.47亿人民币,经营范围为以私募基金从事股权投资、投资管理、资产管理等活动。合伙人信息显示,该基金由中汇人寿保险股份有限公司、上海复星医药产业发展有限公司、弘毅私募基金管理(天津)合伙企业(有限合伙)共同出资。
2026-01-08 17:22
【复星医药:控股子公司药品注册申请获受理】1月8日电,复星医药(600196.SH)公告称,控股子公司复星万邦就丁二酸复瑞替尼胶囊(SAF-189)再次递交药品注册申请获国家药品监督管理局受理,该新药用于间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗。该新药为创新型小分子化学药物,另一适应症非小细胞肺癌(ROS1+)已完成II期临床研究。
2025-12-21 21:27
【三十余家A股上市公司本周披露并购重组最新公告 观想科技筹划购买辽晶电子不低于60%股权明起停牌】12月21日电,据不完全统计,截至发稿,本周(12月15日-12月21日)包括观想科技、金石资源、东方智造、东方雨虹、四川成渝、七一二、天创时尚、中国神华、四川九洲、东方电缆、金达莱、银星能源、旭升集团、中微公司、万隆光电、普路通、联创电子、锋龙股份、美克家居、中金公司、凤形股份、东杰智能、嘉美包装、联合精密、华菱线缆、珈伟新能、皮阿诺、东方园林、百纳千成、中泰化学、TCL科技和复星医药在内的32家A股上市公司披露并购重组进展最新公告。其中,观想科技公告,筹划购买辽晶电子不低于60%股权,股票明起停牌。小财注:截至周五收盘,实控人拟变更为追觅科技创始人俞浩的嘉美包装录得6天4板。
2025-12-19 17:10
【复星医药:控股子公司药品获美国FDA临床试验批准】12月19日电,复星医药(600196.SH)公告称,控股子公司上海复宏汉霖生物技术股份有限公司及其控股子公司获美国FDA批准开展HLX18(重组抗PD-1人源化单克隆抗体注射液)用于治疗多种实体瘤的I期临床试验。复宏汉霖拟于条件具备后于美国开展该药品的I期临床试验。HLX18是复星医药自主研发的纳武利尤单抗生物类似药,拟用于多种癌症的治疗。截至2025年11月,针对HLX18的累计研发投入约为人民币5,253万元。根据美国相关法规要求,HLX18尚需在美国开展一系列临床研究并经美国药品审评部门审批通过后,方可上市。药品研发存在一定风险,敬请广大投资者注意投资风险。
2025-12-16 09:55
医药股震荡下挫,常山药业、一品红跌超10%,金迪克、北大医药、复星医药、联环药业等跟跌。
2025-12-16 08:06
12月16日电,上交所就复星医药对外投资绿谷医药相关事项下发监管工作函,涉及对象为上市公司。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 短线攻略:精准捕捉涨停股票的实战策略
- 股市智慧:精准把握六大卖股时机,稳健增值你的投资
- 增发背后的业绩预期与投资决策
- 补仓技巧深度解析:精准自救,智取股市
- 揭秘股市上涨奥秘:多维度分析股票后期上涨潜力
- 牛市中的金融蓝筹:银行股与保险股的崛起逻辑
- 股市智慧:掌握买卖时机,稳健投资之道
- 股市实战技巧:深入解析T0操作策略
- 洞悉股市主流,精准短线策略
- 炒股避坑指南:识破股市迷雾,稳健前行
- 揭秘股市投资利器:市盈率、市净率与净资产收益率深度解析
- 揭秘股市庄家洗盘策略,掌握盈利先机
- 分红派息策略解析:精准把握四大关键日期
- 应对股市炸板的艺术:策略与低吸战法深度剖析
- 面值退市:股市规则下的企业生死线
- 操盘手的智慧:解码九大生存准则,驾驭金融市场风云
- 股票投资策略:何时减仓与无量上升个股的前景剖析
- 智者投资:买入股票前的十问策略
- 新手股市看盘全攻略:洞悉市场动态,精准把握交易时机
- 揭秘低吸策略:精准捕捉市场机遇的关键要素
当前版本:V3.0

 VIP复盘网
VIP复盘网
