
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
复星医药
600196 |
1.47%
|
最新:22.14
开盘:22.09 昨收:21.82 |
开盘%:1.24%
振幅%:1.24% 换手%:0.45% |
最高:22.28
最低:22.01 量比:1.29 |
总市值:591 亿
流通值:469 亿 成交额:21 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
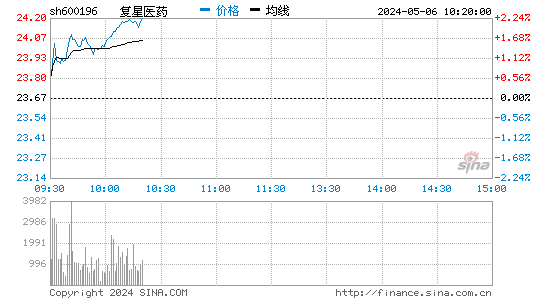
- 分时图
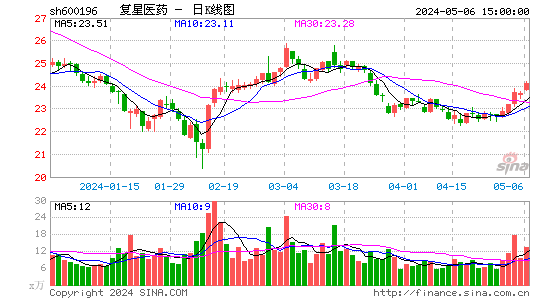
- 日K图
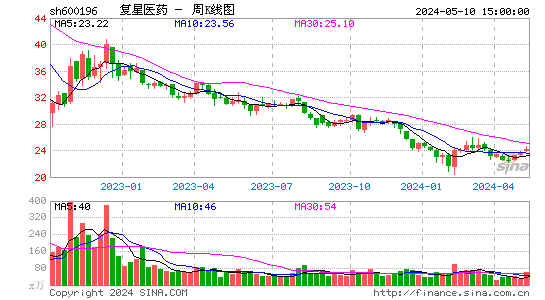
- 周K图
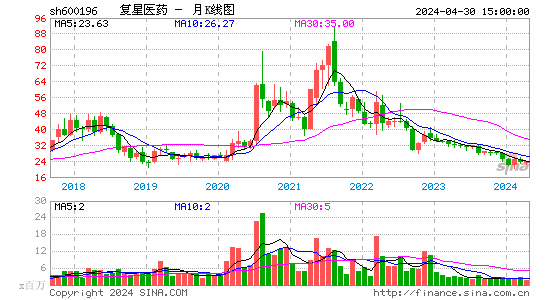
- 月K图
复星医药股票概况
了解全球化医药健康产业集团的股市表现
一、公司概况
复星医药(600196.SH,02196.HK)成立于1994年,是一家植根中国、创新驱动的全球化医药健康产业集团。其业务范围涵盖制药、医疗器械与医学诊断、医疗健康服务等领域,并通过参股国药控股扩展到医药商业领域。
二、股市表现
截至2025年2月10日,复星医药A股收盘价为25.43元,港股收盘价为14.840港元。股价呈现波动性,但整体呈现上升趋势,显示出市场对复星医药的信心。
三、主营业务
制药业务:作为公司的核心业务,包括创新药、成熟产品及制造业务、疫苗业务。其中,创新药业务聚焦肿瘤、免疫等核心治疗领域。
医疗器械与医学诊断:构建以医疗美容、呼吸健康等为核心的三大业务分支。
医疗健康服务:形成线上线下一体化的医疗服务平台。
四、财务状况
复星医药的资产负债率维持在48.64%左右,财务状况稳定。营业收入和归母净利润持续增长,显示出良好的盈利能力和销售毛利率。
五、创新与发展
复星医药在创新药方面增长动能强劲,业务结构持续优化。公司积极推动优质产品出海,不断提升国际声誉和市场份额。
总结
复星医药作为全球化医药健康产业集团的佼佼者,以其稳健的股市表现、多元化的业务布局、良好的财务状况以及持续的创新与发展,赢得了市场和投资者的广泛认可。未来,随着全球医疗健康市场的不断发展,复星医药有望继续保持强劲的增长势头。
2026-06-04 17:08
【复星医药自研创新药FXS0683 I期临床完成首例患者给药】6月4日电,复星医药自主研发的口服小分子创新药FXS0683用于血液系统恶性肿瘤的中国I期临床试验于近日完成首例患者给药。
2026-05-29 16:40
【复星医药:控股子公司帕妥珠单抗注射液获国家药监局批准上市】5月29日电,复星医药(600196.SH)公告称,公司控股子公司复宏汉霖自主研发的帕妥珠单抗注射液(汉倍优®)上市注册申请获国家药品监督管理局批准,适应症覆盖原研药于中国境内已获批的所有适应症,包括早期乳腺癌和转移性乳腺癌。该药品为生物类似药,已获美国FDA和欧盟委员会上市批准,并获加拿大卫生部上市申请受理。截至2026年4月,累计研发投入约2.32亿元。2025年,帕妥珠单抗产品于中国境内销售额约27.28亿元。
2026-05-28 16:48
【复星医药:控股子公司获智翔金泰GR1803双抗许可 总付款上限6亿元】5月28日电,复星医药(600196.SH)公告称,公司控股子公司药友制药与智翔金泰签订许可协议,获授予GR1803双特异性抗体在中国境内及港澳台地区的临床开发、商业化独占权利及生产排他权利,并将作为该产品的上市许可持有人。药友制药将向智翔金泰支付至多6亿元,包括首付款3亿元、上市里程碑2.5亿元及技转里程碑0.5亿元,并基于年度净销售额支付销售里程碑及销售提成。GR1803拟用于治疗多发性骨髓瘤、系统性红斑狼疮等,其附条件上市申请已获国家药监局受理并纳入优先审评。本次许可旨在丰富公司在血液瘤领域的产品管线。
2026-05-26 21:00
【公告精选:深科技子公司拟投资14.7亿元扩大高端存储芯片封测产能;盛视科技子公司签署约60亿元算力产业合作协议】5月26日电,【热点】华塑控股:子公司宏创智能并非从事PCB生产业务。沪电股份:随着PCB行业整体产能持续释放,未来市场竞争预计将会加剧。科瑞技术:目前海外半导体和光模块业务收入规模及营收占比较小。兆易创新:持有长鑫科技股份仅占其当前总股本1.8%,比例较小。宝鼎科技:公司无AI覆铜板,未发现在AI服务器及算力领域应用。恒盛能源:2025年CVD金刚石产品营收占总营收比重为0.15%。力量钻石:“金刚石散热材料”应用场景尚未达到大规模市场化应用阶段。新亚制程:公司业务不涉及半导体设计、制造、封装等。国晟科技:异质结(HJT)组件应用领域未发生重大变化。晶方科技:拟将境外控股子公司Anteryon分拆至阿姆斯特丹交易所上市。深科技:子公司拟投资14.7亿元扩大高端存储芯片封测产能。盛视科技:子公司签署算力产业合作协议,业务体量折算约60亿元。柏诚股份:拟定增募资不超12亿元,用于高科技产业专项工程建设项目。林州重机:因涉嫌信息披露违法违规被证监会立案。【并购重组】富创精密:拟1.89亿元收购上海日扬65%股权。同仁堂:控股子公司同仁堂商业终止对红惠医药投资。仕佳光子:终止购买东莞福可喜玛通讯科技公司股权事项。倍杰特:终止收购文冶有色控股权,子公司拟取得金鑫冶金55%股权。复星医药:控股子公司拟4.14亿元取得肝病创新药企业星曜坤泽20.87%股权。【中标合同】奥来德:中标4369.54万元绵阳京东方PNL工厂技术升级改造项目。金固股份:再次获头部新能源汽车主机厂阿凡达低碳车轮项目定点。中国通号:3—4月中标五个重要项目,中标总额约9亿元。中油工程:1—4月新签合同额718.15亿元,同比增长69.91%。【增减持&回购】木林森:实控人拟1亿元至1.5亿元增持公司股份。杰瑞股份:董事长、副总裁拟合计800万元至1000万元增持公司股份。ST易购:部分董事、高管及核心骨干拟合计不低于600万元增持股份。海螺水泥:拟6亿元至10亿元回购A股股份。亚世光电:控股股东、高管及股东拟合计减持公司不超5.28%股份。永安期货:浙江东方拟减持公司不超3%股份。芯联集成:员工持股平台拟合计减持公司不超0.33%股份。恒光股份:湘江投资及公司高管拟合计减持不超3%股份。燕东微:亦庄国投拟减持公司不超1%股份。超达装备:青岛海青拟减持公司不超1%股份。先锋精科:优立佳合伙拟减持公司不超3%股份。安凯客车:安徽省投资集团拟减持公司不超1%股份。【其他】佰维存储:子公司拟1亿元参设产业基金,围绕存储+先进封装领域布局。天赐材料:开展年产16万吨高压实磷酸铁锂项目前期工作。沧州大化:聚海分公司生产装置检修完成,恢复生产。广电计量:拟公开发行公司债券不超10亿元。
2026-05-26 17:01
【复星医药:拟出资4.14亿元参与肝病创新药公司星曜坤泽B轮融资及股权转让】5月26日电,复星医药(600196.SH)公告称,公司控股子公司复星医药产业拟出资共计4.14亿元参与星曜坤泽B轮融资并受让联营公司苏州基金、天津基金所持部分股权。其中,拟出资2.18亿元认缴星曜坤泽293.68万元新增注册资本,拟出资1.97亿元受让苏州基金、天津基金所持合计308.65万元存续注册资本。交易完成后,复星医药产业将持有星曜坤泽20.87%股权。标的公司主要从事肝病创新药物的研究和开发。本次投资构成关联交易,旨在丰富公司在肝病治疗领域的管线布局。
2026-05-21 16:48
【复星医药:控股子公司药品左氧氟沙星注射液获注册批准】5月21日电,复星医药(600196)5月21日公告,近日,公司控股子公司重庆药友制药有限责任公司就左氧氟沙星注射液的药品注册申请获国家药品监督管理局批准。本次获批适应症为用于敏感细菌所引起的下列轻、中、重度感染:(1)医院获得性肺炎;(2)社区获得性肺炎;(3)急性细菌性鼻窦炎;(4)慢性支气管炎的急性细菌性发作;(5)复杂性皮肤及皮肤结构感染;(6)非复杂性皮肤及皮肤软组织感染;(7)慢性细菌性前列腺炎;(8)复杂性尿路感染;(9)急性肾盂肾炎;(10)非复杂性尿路感染;(11)吸入性炭疽(暴露后)。
2026-05-21 16:38
【复星医药:控股子公司药品HLX48获临床试验批准】5月21日电,复星医药(600196.SH)公告称,公司控股子公司复宏汉霖收到国家药监局批准,同意注射用HLX48(靶向EGFR和c-MET的抗体偶联药物)用于晚期/转移性实体瘤治疗开展Ⅰ期临床试验。截至公告日,于全球范围尚无靶向EGFR和c-MET的双特异性抗体偶联药物获批上市。
2026-05-21 16:38
【复星医药:控股子公司HLX3902注射液获准在澳大利亚开展临床试验】5月21日电,复星医药(600196.SH)公告称,公司控股子公司复宏汉霖自主研发的HLX3902注射液(STEAP1xCD3xCD28三特异性抗体)用于转移性去势抵抗性前列腺癌及其他晚期实体瘤治疗的Ⅰ期临床试验方案,已获澳大利亚药品管理局备案及伦理委员会批准,系该药品全球首个临床试验许可。截至公告日,于全球范围尚无靶向STEAP1、CD3及CD28的三特异性抗体产品获批上市。
2026-05-20 14:11
【袁春出任安科生物联席CEO兼首席商务官】5月20日电,5月20日,安科生物正式宣布,前复星全球合伙人、复星医药国内营销平台副董事长、复星医药国内营销平台CEO袁春加盟公司,出任联席CEO兼首席商务官,全面负责安科生物销售管理、营销体系运营及产品品牌价值建设。
2026-05-13 20:29
【公告精选:通鼎互联称与英伟达不存在任何业务关系;腾讯一季度收入同比增9%】5月13日电,【热点】通鼎互联澄清:与英伟达不存在任何业务关系六连板大唐发电:截至目前,公司尚无已投运算电协同项目3天2板中船特气:部分下游客户就六氟化钨产品与公司业务洽谈增加 但目前尚未签署新的长期或大额实质性订单协议2连板可川科技:子公司可川光子主营业务暂未形成营收普冉股份:公司主营产品利基型非易失性存储产品对应的市场规模相对较小太极实业:控股子公司海太半导体(无锡)有限公司2025年度完成营收39.39亿元【再融资】中材国际:公开发行不超20亿元公司债券获证监会同意注册批复神工股份:拟定增募资不超10亿元 用于硅零部件扩产等项目拓新药业:拟定增募资不超2.28亿元【增减持、回购】泰格医药:拟5亿元至10亿元回购股份泉阳泉:控股股东拟1750万元—3500万元增持公司股份森泰股份:控股股东及实控人拟600万元至1200万元增持股份德福科技:股东拟减持不超3%公司股份泰嘉股份:控股股东拟减持公司不超3%股份北纬科技:实控人拟减持公司不超3%股份浙江东方:拟出售已回购股份信隆健康:控股股东拟减持公司不超1%股份汇嘉时代:控股股东拟减持不超1%公司股份通源石油:副董事长张志坚拟减持不超0.14%公司股份【经营数据】腾讯控股:一季度收入1964.58亿元 同比增长9%阿里巴巴:一季度收入2433.8亿元 同比增长3%新城控股:4月商业运营总收入约11.71亿元 同比增长3.17%中原高速:4月份通行费收入为3.57亿元赣粤高速:4月份车辆通行服务收入约2.81亿元【中标合同】易普力:中标合计约16.94亿元项目华秦科技:签订航空发动机用特种功能材料销售框架协议 总金额上限为14.8亿元宁波建工:全资子公司中标9.45亿元项目国机汽车:全资子公司签署1.09亿元经营合同金固股份:收到两份阿凡达低碳车轮项目定点通知平治信息:子公司预中标约5823.87万元中国移动采购项目【重大投资】中国巨石:拟44.31亿元建设年产5万吨电子纱暨3.2亿米电子布生产线项目恩捷股份:拟投建年产50亿平方米锂电池隔离膜项目 预计总投资额为40亿元深圳燃气:拟不超24.24亿元投建大朗电厂项目瑞可达:拟对联营企业苏州瑞创增资3500万元【其他】广联航空:拟3.57亿元收购天津跃峰51%股权奥翔药业:参股公司英派药业在香港联交所主板挂牌上市博威合金:拟出售美国太阳能业务电池资产禾丰股份:部分控股子公司进项税金转出、补缴税费及滞纳金佰维存储:重新向香港联交所递交H股发行并上市申请复星医药:控股子公司与AriBio签订独家选择权协议诺诚健华:ICP-054(ZB021)完成首例受试者入组迪哲医药:血液瘤产品高瑞哲®和比瑞替尼研究成果入选2026年欧洲血液学协会年会金城医药:戊酸雌二醇化学原料药上市申请获批恒瑞医药:SHR-3821注射液等三款药品获批临床试验北陆药业:盐酸达克罗宁化学原料药上市申请获批太极集团:二甲双胍恩格列净片(Ⅰ)获得药品注册证书ST人福:盐酸R-氯胺酮注射液药物临床试验获批准
2026-05-10 15:33
【复星医药:斯鲁利单抗注射液新增适应症获欧盟批准】5月10日电,复星医药(600196.SH)公告称,公司控股子公司复宏汉霖自主研发的斯鲁利单抗注射液新增两项适应症获欧盟委员会批准,分别为联合化疗一线治疗PD-L1CPS≥5的不可切除局部晚期、复发或转移性食管鳞状细胞癌成人患者,以及联合化疗一线治疗EGFR基因突变阴性、ALK或ROS1阴性的不可手术切除局部晚期或转移性非鳞状非小细胞肺癌成人患者。该药品此前已在欧盟获批用于广泛期小细胞肺癌一线治疗。本次获批将强化该药品在国际市场布局,但具体销售情况受多重因素影响,存在不确定性。
2026-05-08 16:29
【复星医药:控股子公司盐酸文法辛缓释片获注册批准】5月8日电,复星医药(600196.SH)公告称,公司控股子公司复星医药(徐州)有限公司的盐酸文法辛缓释片药品注册申请获国家药监局批准,用于治疗抑郁症及广泛性焦虑障碍。该药品为自主研发的化学药品,截至2026年4月累计研发投入约768万元。2025年,同类药品于中国境内销售额约5.84亿元。本次获批将进一步丰富公司产品剂型,但销售情况受多重因素影响,存在不确定性。
2026-04-30 20:27
【公告精选:江淮汽车拟投资引望智能技术有限公司;五粮液拟以80亿元—100亿元回购公司股份】4月30日电,【热点】三连板宝光股份:2025年宝光联悦氦气业务营业收入为91.8万元,氦气为配套气体业务,占比很小。四连板越剑智能:智能验布机产品仍在市场推广的前期阶段。德方纳米:股票交易异常波动,公司目前经营情况未发生重大变化。舒华体育:股票交易异常波动,未涉及市场热点概念。金瑞矿业:主要原材料天青石若延续涨价趋势,将对公司经营业绩产生不利影响。日联科技:购买上海菲莱测试技术有限公司100%股权事项尚处于筹划阶段。【业绩】广州港:4月预计完成货物吞吐量5108.4万吨,同比增长1.2%。五粮液:2025年净利润89.54亿元同比下降71.89%,拟10派25.78元。五粮液:第一季度净利润同比增长82.57%。【增减持】天岳先进:股东拟合计减持不超2.2%公司股份。神奇制药:控股股东的一致行动人拟减持不超2.69%公司股份。兰剑智能:股东拟减持不超1%公司股份。路德科技:股东及部分高管拟合计减持不超1.5466%公司股份。天通股份:实控人的一致行动人拟合计减持不超1.56%公司股份。联合水务:股东拟减持不超3%公司股份。瑞斯康达:股东拟减持不超1.95%公司股份。上海港湾:控股股东拟减持不超过3%公司股份。【回购】汇川技术:回购公司股份34.20万股,成交总金额2228万元。宏华数科:回购股份82.47万股,成交总金额为4974万元。五粮液:拟以80亿元—100亿元回购公司股份。【合同中标】友讯达:中标约1.69亿元国家电网采购项目 金额占公司2025年经审计营业收入21.16%。福龙马:4月预中标的环卫服务项目数3个。三星电气:预中标约3.49亿元国家电网项目。万胜智能:预中标2.2亿元国家电网项目。【股权变动】航天机电:拟挂牌转让连云港新能源81.7552%股权。湖南海利:拟参与丰乐农化51%股权公开竞价。德林海:控股股东等拟协议转让14.97%公司股份;受让方承诺不会与上市公司开展AI眼镜业务。龙元建设:控股股东终止筹划控制权变更事项。【重大投资】江淮汽车:公司拟投资引望智能技术有限公司。【并购重组】中芯国际:上交所并购重组审核委员会定于5月11日审议公司发行股份购买资产暨关联交易事项。【再融资】新澳股份:拟定增募资不超10.19亿元,用于新澳越南高档精纺生态纱纺织染整项目(二期)等。信科移动:拟定增募资不超70亿元,用于空天地一体化移动通信产业化项目等。*ST八钢:拟向华宝投资定增募资12.97亿元。【其他】沧州大化:聚海分公司生产装置停产检修。巨人网络:收到重庆证监局行政监管措施决定书,因公司未按规定就相关交易履行关联交易审议程序及信息披露义务。S佳通:因涉嫌信息披露违法违规,证监会决定对公司立案。百利电气:公司董事长变更为张建新。复星医药:硝普钠注射液获药品注册批准。善水科技:全资子公司长兴化工停产。长久物流2026年中期利润分配预案:拟10派3.4元。江西铜业:筹划控股子公司江铜铜箔分拆上市。昊海生科:控股股东蒋伟因非本公司事项收到《取保候审决定书》。卓然股份:无法在法定期限内披露《2025年年度报告》,股票停牌。科蓝软件:因涉嫌信息披露违法违规,中国证监会决定对公司进行立案。
2026-04-30 16:32
【复星医药:硝普钠注射液获药品注册批准】4月30日电,复星医药(600196)4月30日公告,控股子公司重庆药友制药有限责任公司就硝普钠注射液的药品注册申请获国家药品监督管理局批准。本次获批适应症为(1)高血压急症,如高血压危象、高血压脑病、恶性高血压、嗜铬细胞瘤手术前后阵发性高血压等的紧急降压,也可用于外科麻醉期间进行控制性降压;(2)急性心力衰竭,包括急性肺水肿,亦用于急性心肌梗死或瓣膜(二尖瓣或主动脉瓣)关闭不全时的急性心力衰竭。
2026-04-29 11:38
【第三批上海市创新型企业总部授牌仪式举行】29日讯,第三批上海市创新型企业总部授牌仪式今日举行。此次授牌的企业共有44家,覆盖集成电路、生物医药、人工智能、数字经济等战略性新兴产业重点领域,包括复星医药、禾赛科技、骄成超声等。
2026-04-29 10:09
【港股创新药板块多数调整,泰格医药跌超9%】港股创新药板块多数调整,泰格医药跌超9%,凯莱英、昭衍新药跌超4%,荣昌生物、复星医药跟跌。
2026-04-14 17:38
【复星医药:控股子公司HLX05-N注射液临床试验获批】复星医药4月14日公告,公司控股子公司上海复宏汉霖生物技术股份有限公司及其控股子公司收到国家药品监督管理局关于同意HLX05-N(即重组抗EGFR人鼠嵌合单克隆抗体注射液)用于转移性结直肠癌治疗开展Ⅰ期临床试验的批准。HLX05-N系集团自主研发的西妥昔单抗注射液生物类似药,拟用于转移性结直肠癌及头颈部鳞状细胞癌治疗。
2026-04-14 16:46
【复星医药:控股子公司FKC289注射液获临床试验批准】4月14日电,复星医药(600196.SH)公告称,公司控股子公司复星凯瑞收到国家药监局关于同意FKC289注射液开展I/II期临床试验的批准。该药品为靶向BCMA和CD19的基因修饰CAR-T细胞产品,拟用于复发/难治原发性轻链淀粉样变及复发/难治膜性肾病的治疗。截至2026年3月,集团针对该药品的累计研发投入约为0.59亿元。目前全球尚无同一分子机制的治疗产品获批上市。鉴于药品研发存在不确定性,后续尚需完成临床研究并经审批通过方可上市,敬请投资者注意投资风险。
2026-04-10 16:29
【复星医药:控股子公司氟比洛芬酯注射液获注册批准】4月10日电,复星医药(600196.SH)公告称,公司控股子公司重庆药友制药有限责任公司的氟比洛芬酯注射液注册申请获国家药品监督管理局批准,适应症为用于术后及癌症的镇痛。该药品为集团自主研发的化学药品3类,截至2026年3月,累计研发投入约0.34亿元。数据显示,2025年氟比洛芬酯注射液在中国境内销售额约11.58亿元。此次获批将进一步丰富公司产品线。
2026-04-09 17:21
【复星医药:控股子公司获药品补充申请批准】4月9日电,复星医药(600196.SH)公告称,公司控股子公司复宏汉霖自主研发的汉利康®(利妥昔单抗注射液)新增适应症的补充申请获国家药监局批准。本次新增适应症包括:联合维泊妥珠单抗等药物治疗既往未经治疗的弥漫大B细胞淋巴瘤(DLBCL)成人患者;联合苯达莫司汀和维泊妥珠单抗治疗不适合接受造血干细胞移植的复发或难治性DLBCL成人患者。
2026-04-07 13:52
【复星医药在珠海成立医药科技公司】4月7日电,企查查APP显示,近日,珠海星韬医药科技有限公司成立,法定代表人为关晓晖,注册资本为1000万元,经营范围包含:医学研究和试验发展;财务咨询;信息技术咨询服务;品牌管理;企业总部管理等。企查查股权穿透显示,该公司由复星医药间接全资持股。
2026-04-02 16:52
【复星医药:首席财务官变更】4月2日电,复星医药(600196.SH)公告称,公司近日收到陈战宇的辞职函,因工作安排调整,其辞去首席财务官职务,自2026年4月2日生效,辞任后仍担任高级副总裁。同日,董事会同意聘任黄智为公司高级副总裁、首席财务官。
2026-04-01 16:45
【复星医药:控股子公司HLX319获临床试验批准】4月1日电,复星医药(600196.SH)公告称,公司控股子公司复宏汉霖近日收到国家药监局批准,同意其自主研发的HLX319(帕妥珠曲妥珠单抗注射液)用于HER2阳性早期或局晚期乳腺癌新辅助治疗开展Ⅰ期临床试验。该药物拟用于早期乳腺癌的辅助╱新辅助治疗与转移性乳腺癌的治疗。
2026-04-01 15:58
【复星医药等在天津成立创业投资基金,出资额10亿】天眼查App显示,近日,天津复星海河医疗健康产业二期创业投资基金合伙企业(有限合伙)成立,执行事务合伙人为星耀二号(天津)企业管理合伙企业(有限合伙),出资额10亿人民币,经营范围为创业投资,以私募基金从事股权投资、投资管理、资产管理等活动。合伙人信息显示,该基金由天津市海河产业基金合伙企业(有限合伙)、复星医药旗下苏州君明致远创业投资合伙企业(有限合伙)、天津港保税区产业发展基金合伙企业(有限合伙)等共同出资。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 掌握价值投资精髓:三大策略助力战胜市场
- 股市下跌时应避免的七大错误行为
- 深度解析搓揉线:识别上涨中继洗盘与高位出货的关键信号
- 深度解析龙头战法复盘精髓,精准捕捉股市脉搏
- 警惕诱多陷阱:揭秘五种典型庄家手法
- 股市高手的炒股智慧:口诀引领投资之道
- 揭秘股市雷区:七大类型股票碰不得
- 新股民的生存法则:股市十二条军规深度解析
- 主力操盘揭秘:低位吸筹到高位派发的全链条解析
- 散户追逐涨停板的策略与风险控制
- 弱市中的选股策略:重个股,轻大盘
- 股市出货八大黄金法则深度解析
- 揭秘龙头战法:精准捕捉市场明星股的艺术
- 揭秘股市迷雾:为何我们常常与翻倍股擦肩而过?
- 混沌期股市策略:精准捕捉板块轮动,稳健前行
- 揭秘股债联动:高效可转债交易策略深度剖析
- 创业板三年梦碎:股民亏损与富豪套现的鲜明对比
- 逆向投资策略:股市中的稳健之选
- 揭秘股市庄家洗盘策略,掌握盈利先机
- 美联储不加息助推股市反弹,A股迎利好但缺口压力仍存
当前版本:V3.0

 VIP复盘网
VIP复盘网
